成纖維細胞生長因子(FGFs)家族由22個成員組成🤸🏻♂️,是最大的生長因子家族。在成人組織中FGFs通過重新激活發育信號通路來介導代謝功能,組織修復和再生,並參與維持多種關鍵的生物學功能,包括細胞生長和分化,血管生成,胚胎發育,傷口愈合修復以及細胞的代謝調節等。在吸煙肺鱗癌(S-LSCC)中FGF19💣、FGF3🏠、FGF4和CCND1區域的擴增頻率是非吸煙者肺鱗癌(NS-LSCC)中的5倍,並在獨立的LSCC臨床樣本中驗證了FGF19的擴增。進一步地,FGF19在體外可以促進LSCC細胞的增殖,這些數據表明FGF19是吸煙肺鱗癌病人中潛在的驅動基因。在此基礎上,意昂4体育平台夏偉梁教授課題組繼續探究驅動基因FGF19及其主要受體FGFR4促進LSCC進展的潛在機製🥷🏼。研究者發現吸煙或化療可引起內質網應激📲,並進一步促進FGF19在肺癌細胞中的惡性上調。針對高表達FGF19的LSCC👉🏽,該課題組首次報道了使用AZD2014抑製腫瘤中mTOR通路是可行的☀️。這些發現為在FGF19驅動的LSCC中通過靶向抑製FGF19/ FGFR4通路或直接使用基於mTOR通路的治療提供了新的策略🐵🐜。該論文於2020年2月28日發表在Nature旗下腫瘤學期刊Oncogene上 [2]🚵🏽♀️🖐。

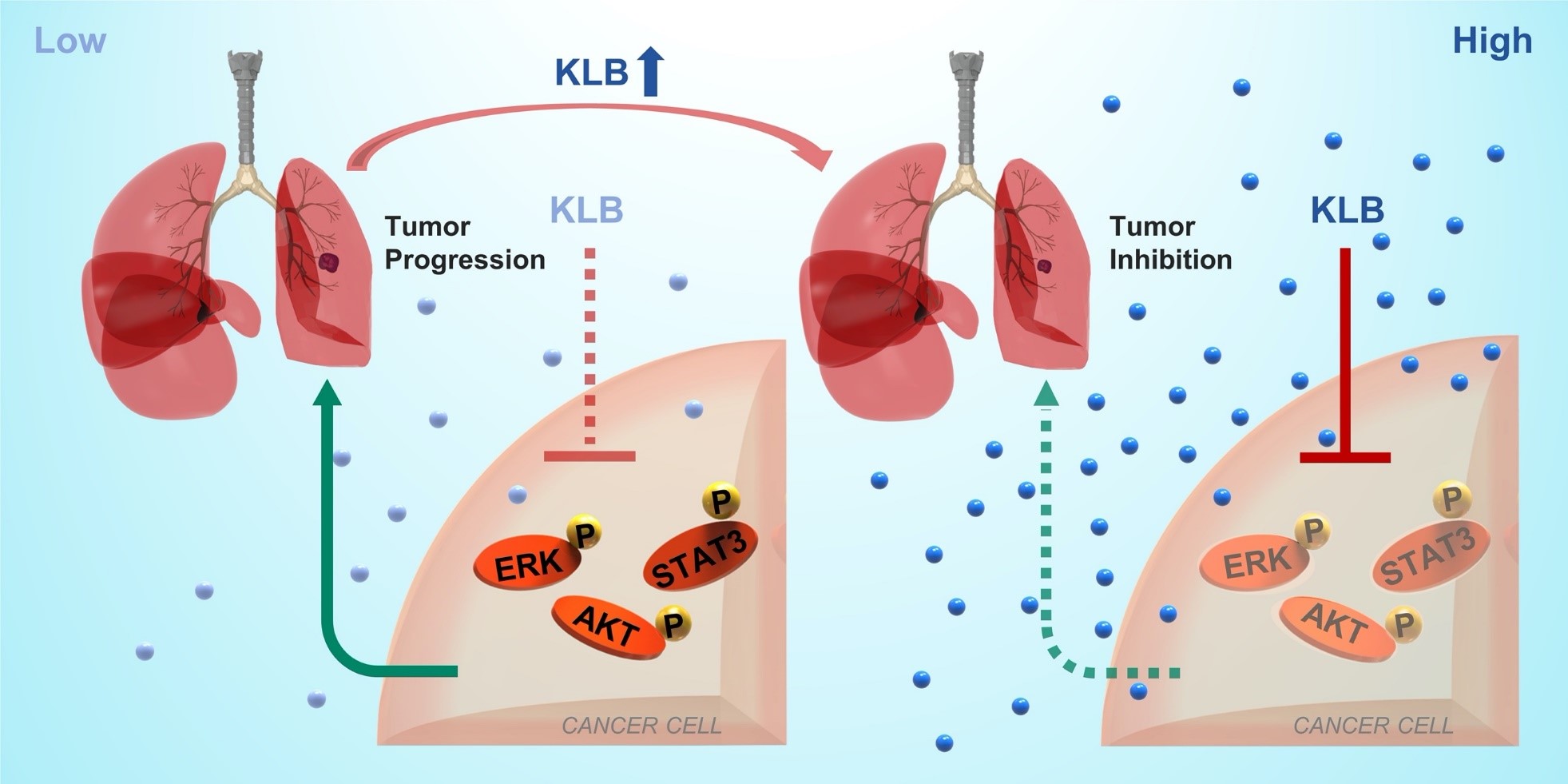
FGF19是一個內分泌型生長因子🥑,其與特異性受體FGFR4結合需要借助Klotho家族蛋白中的KLB(βKlotho)形成FGF19-KLB-FGFR4復合體激活下遊的多種信號通路途徑,影響血管生成,細胞分化等多種生物過程🐬。β-Klotho屬於Klotho家族,在細胞能量代謝,細胞衰老和肌肉再生等方面起重要作用。由於過表達Klotho家族中α-Klotho可以顯著延長小鼠壽命🙆🏻♀️,α-Klotho被公認為抗衰老基因👩❤️💋👨。此外,已有研究表明,在癌組織中,α-Klotho的啟動子區域易發生高甲基化🦸🏼,導致其表達降低🧖🏿♀️,但通過過表達α-Klotho可抑製多種癌症的發生和發展🏋🏿♂️🚣🏻♂️。在氨基酸序列上β-Klotho與α-Klotho具有41%的相似性,但FGF19的共受體βKlotho在非小細胞肺癌中的作用機製尚不清楚。在研究過程中,夏偉梁課題組進一步通過大量臨床切片樣本,對比了非小細胞肺癌的癌組織和癌旁組織樣本中β-Klotho的表達量以及腫瘤病人和正常人的血清β-Klotho含量🧝🏿,探討了其作為診斷/預後生物標誌物的臨床意義。研究發現👳🏽♂️,β-Klotho在腫瘤組織中低表達🐢,可以作為輔助診斷非小細胞肺癌的指標。本項研究還測試了β-Klotho在荷瘤小鼠體內外的作用😚。利用多種小鼠模型(原位模型及皮下瘤模型)以及細胞實驗🙆🏽♀️,研究者發現,外源性β-Klotho給藥或過表達β-Klotho可以促進細胞凋亡和細胞周期阻滯👨👦👰🏻♀️,同時伴隨著ERK1/ 2,AKT和STAT3信號的失活,抑製非小細胞肺癌細胞的增殖和轉移🖐🏼👩👩👦👦。這表明β-Klotho在非小細胞肺癌中具有潛在的診斷/治療價值。此外,通過多種數據庫數據驗證🙇🏻♀️,發現β-Klotho的表達量與淋巴結轉移,總體生存和無進展生存有負相關關系。課題組認為βKlotho可作為NSCLC治療的潛在新靶標🅰️,在未來有一定的臨床應用🍪。關於β-Klotho的工作已於2019年10月發表在診療學知名期刊Theranostics上。
這兩項研究獲得了國家自然科學基金委面上基金、意昂4平台醫工交叉重點和面上等項目的支持,夏偉梁教授為這兩項研究的通訊作者,博士生李凡為第一作者🙅🏻♀️。該系列研究也是夏偉梁團隊和意昂4平台附屬胸科醫院陸舜主任團隊自2013年在Lung Cancer發表第一篇合作論文以來的第10篇論文🧗🏿♂️。前期雙方合作🔀,已在Oncogene、Cancer Letters等腫瘤學期刊發表了共同通訊論文6篇🏫。主要發現了(1)FGFR1通過Hedgehog信號通路調節肺鱗癌幹細胞表型的分子機製,提出FGFR1和Hedegehog中GLI2的抑製劑聯用治療肺鱗癌(Oncotarget,2016);(2)發現了FGFR1與Hippo/YAP信號通路互作調控肺癌轉移和幹性表型🙅🏻,解釋了臨床上應用FGFR1作為診斷標誌物的理論基礎(Cancer Lett, 2018);(3)FGFR信號還參與調控肺癌細胞自噬(J Exp Clin Cancer Res,2017)以及FGFR1-ERK1/2-SOX2信號軸調控肺癌細胞上皮間質轉化和轉移(Oncogene,2018)。這些工作揭示了FGFs-FGFRs信號調控的復雜性👨🏼🔧,以及同時幹預下遊靶點在臨床上應用的基礎🚵🏻♀️。最近的這兩項工作是在發現FGF/FGFR信號軸在肺癌中作用的基礎上開展後續深入研究的成果。
原文鏈接🧑🏽🎤:
1. https://www.nature.com/articles/s41388-020-1227-2
2. https://www.thno.org/v09p7474.htm
1. Li F, Li Z, Han Q, Cheng Y, Ji W, Yang Y, Lu S, Xia W*. Enhanced autocrine FGF19/FGFR4 signaling drives the progression of lung squamous cell carcinoma, which responds to mTOR inhibitor AZD2104. Oncogene 2020 Feb 28. doi:10.1038/s41388-020-1227-2.
2. Li F, Li X, Li Z, Ji W, Lu S, Xia W*. βKlotho is identified as a target for theranostics in non-small cell lung cancer. Theranostics. 2019; 9:7474-7489.