卒中(stroke)是我國排在第一的高致死高致殘的疾病,嚴重危害了人類的生命健康🤚。近年來的臨床上應用藥物溶栓和機械取栓治療急性缺血性卒中,患者死亡率大大降低💽,但存活的患者卻存在不同程度甚至十分嚴重的神經功能障礙。闡明神經功能障礙的分子病理機製🌉,改善卒中病人預後,是全世界正在努力攻克的一個科學難題。
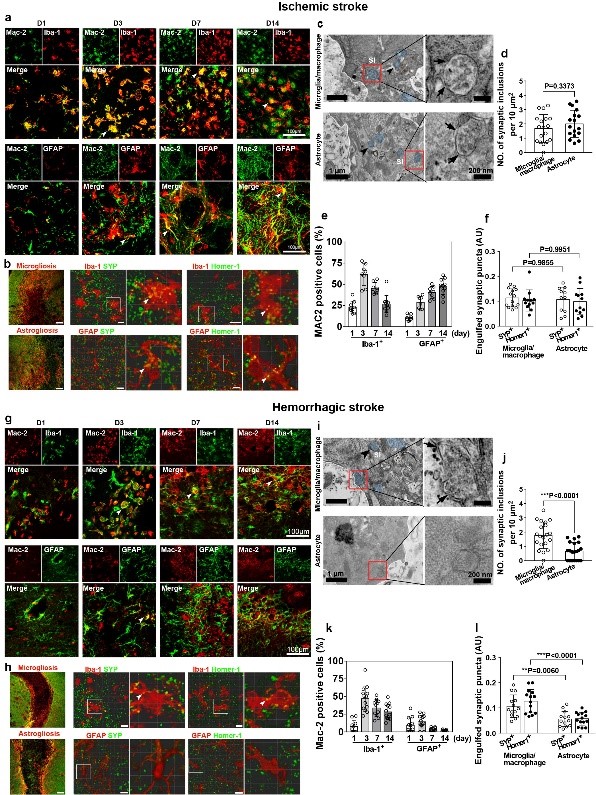
反應性膠質細胞在不同卒中類型中的吞噬功能差異
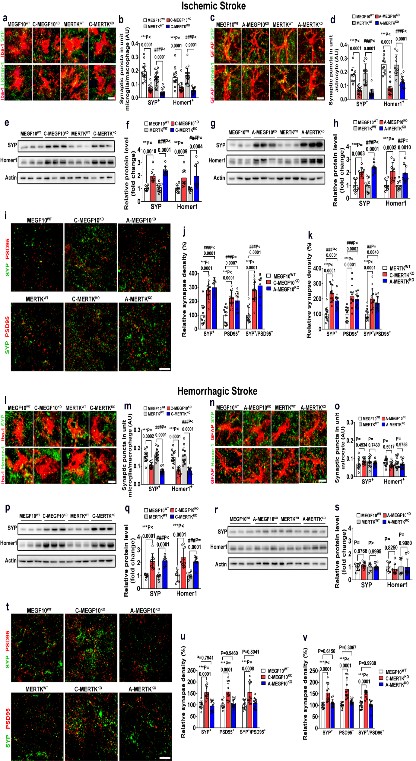
抑製膠質細胞吞噬促進了腦損傷區突觸密度
近日,意昂4体育平台楊國源教授課題組在Nature Communications發表了題為“Stroke-subtype dependent synapse elimination by reactive gliosis in mice”的研究工作👤。該工作利用嚙齒類動物腦血管疾病模型,探索小膠質細胞/巨噬細胞(microglia/macrophage)和星形膠質細胞(astrocyte)在缺血性卒中和出血性卒中修復階段的突觸吞噬情況。研究發現兩種膠質細胞在腦缺血(ischemic stroke)小鼠中過度激活從而吞噬神經突觸,使得突觸丟失影響了疾病預後;而在腦出血小鼠中只有小膠質細胞/巨噬細胞過度激活介導突觸吞噬🗻,星形膠質細胞無明顯作用🧫。采用條件性基因敲除小鼠🧎♂️➡️🏨。通過免疫電鏡、高爾基染色等技術證明了反應性膠質細胞是通過MEGF10/MERTK吞噬通路對膠質增生區域的突觸前膜和後膜進行吞噬。單細胞測序分析進一步發現了與缺血性卒中相比🦶🏿,出血性卒中後介導神經突觸吞噬的星形膠質細胞亞群數量明顯降低。所有這些結果都提示了在卒中修復期,膠質細胞可通過MEGF10和MERTK這兩個關鍵分子吞噬神經突觸𓀍,導致神經突觸丟失和神經環路破壞,最終造成神經功能障礙。
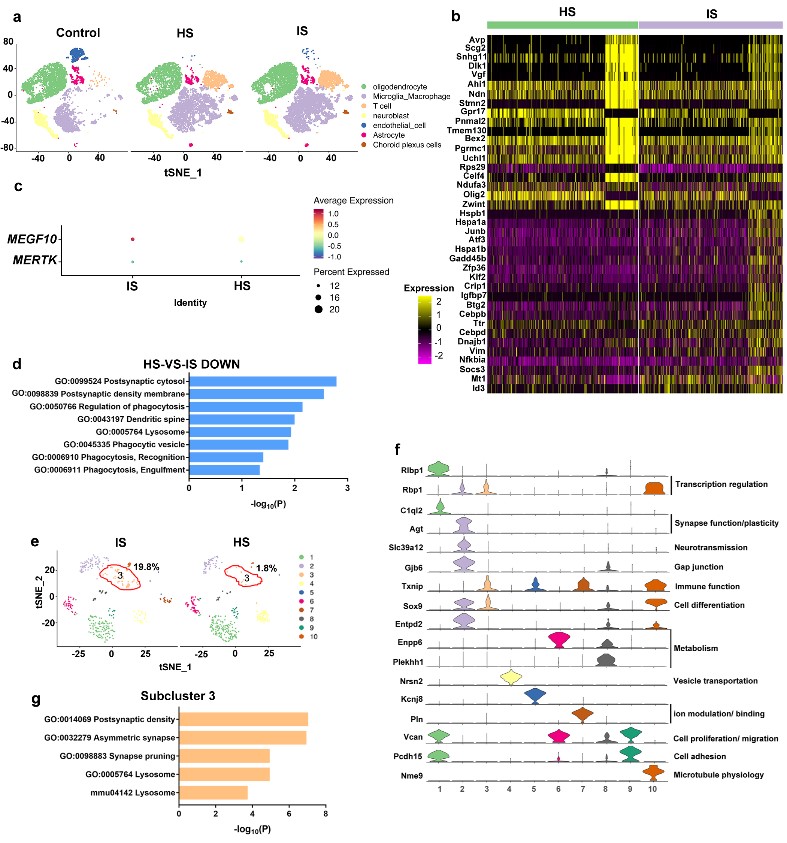
腦出血後介導突觸吞噬的星形膠質細胞亞群數量減少
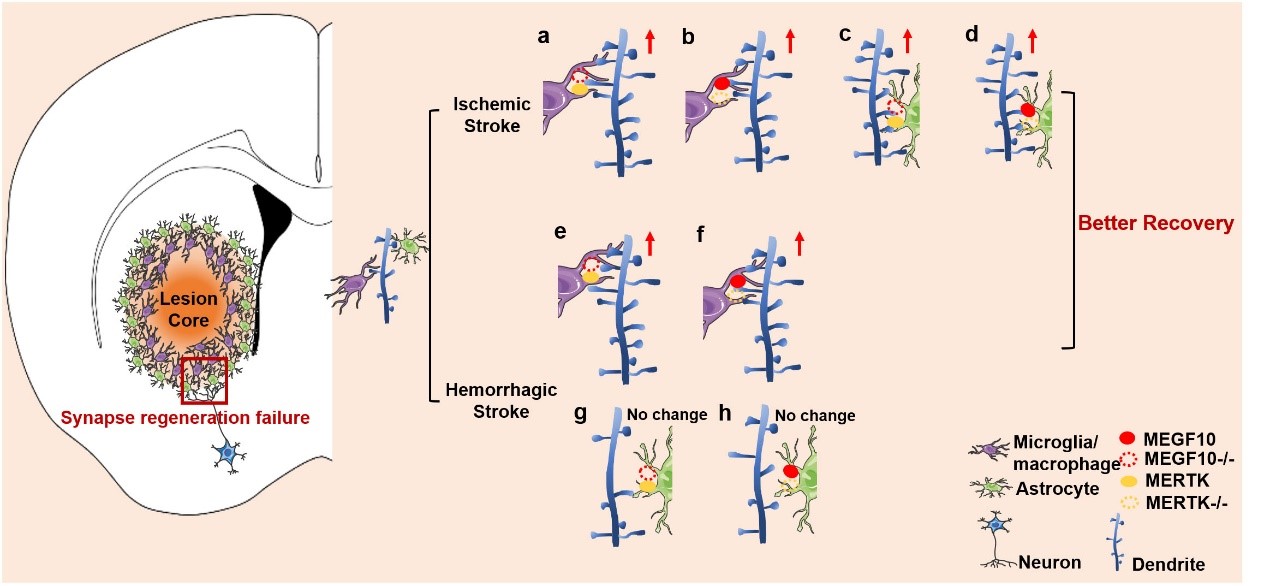
腦損傷後的神經突觸再生和神經網絡重塑是神經損傷修復的關鍵🐰🥮,在卒中後1-2周,神經突觸再生到達峰值,此時活化增殖的膠質細胞可形成反應性膠質增生區域;膠質增生對於神經突觸再生是有益還是有害的,一直都是充滿爭議的科學問題。楊國源團隊的研究證明了小膠質細胞和星形膠質細胞可通過吞噬作用造成神經突觸丟失🤾🏿♀️;而抑製膠質細胞吞噬能顯著增加損傷周邊區的神經突觸密度𓀓,減輕小鼠腦損傷🧑🏿🚒,改善小鼠的運動和認知功能。鑒於小膠質細胞和星形膠質細胞在不同卒中類型中介導突觸吞噬的差異性,針對不同腦損傷病理階段,開發精準有效治療策略,將大大促進腦血管病的預後👨🏼🦰。
意昂4体育平台博士生施曉婧、碩士生羅龍龍(現在瑞典KTH攻讀博士)、意昂4平台醫意昂4附屬瑞金醫院康復醫學科主治醫生王繼先博士為論文的共同第一作者,韓國科學技術院助理教授Won-Suk Chung、意昂4体育平台助理教授湯耀輝和講席教授楊國源為論文的共同通訊作者。該研究工作得到了國家科技部、自然科學基金委🌞、上海市科學技術委員會、上海市教育委員會等項目的支持。
供稿單位:科研與學科辦
作者♟:陶麗寧💙、黃娟娟
審核👨🏻💼:古宏晨
