癌細胞在腫瘤的發生和發展過程中經歷代謝重編程🧹,以滿足其增加的生物能量和生物合成需求,並減輕癌細胞增殖和存活所需的氧化應激,形成了具有葡萄糖成癮和高抗氧化水平的腫瘤微環境,給癌症治療造成了的極大的阻礙。針對腫瘤微環境獨特的代謝特征🧑🏼🍼🪡,各種新興治療策略🐗,如饑餓療法、光動力療法和化學動力療法,已經引起了廣泛的研究並取得明顯的進展。然而🤵🏻♀️🏄🏿,由於惡性腫瘤的代謝靈活性和可塑性🦕,使其在不利條件下獲得生存優勢🦂,抵抗大多數類型的抗癌治療🙇🏿。因此,調控腫瘤的這種代謝靈活性和可塑性可能是提高腫瘤傳統治療療效的一種有效的策略👩🏻🔬👰🏼♂️。
基於此,近日意昂4体育平台張春富課題組聯合錢昆教授團隊在《Advanced Functional Materials》期刊上發表了題為“A Self-Enhancing Nanoreactor Reinforces Radioimmunotherapy by Reprogramming Nutrients and Redox Metabolisms”的文章(2023, 2212510. https://doi.org/10.1002/adfm.202212510)👨🏼🌾。該研究利用金屬基納米材料的類酶催化特性🗣,製備了集成四種類酶活性的多金屬介孔納米顆粒(PdPtAu@TF MNPs),並將其成功應用於腫瘤代謝重編程和增強放射免疫治療中(圖1)。
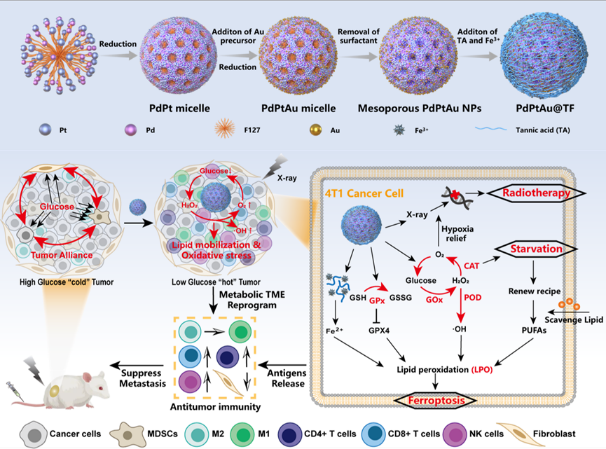
圖13️⃣:PdPtAu@TF納米顆粒的合成及代謝調節示意圖
通過表面活性劑導向法設計合成了Pd/Pt/Au三金屬介孔納米顆粒👰🏿♀️,並以具有pH響應性的單寧酸-鐵離子(FeIIITA)金屬-有機聚合物表面塗敷。酶催化性質測試結果表明,PdPtAu MNPs具有類葡萄糖氧化酶(GOx-mimic)🤽🏼♀️🦂、類過氧化氫酶(CAT-mimic)、類過氧化物酶(POD-mimic)和類谷胱甘肽過氧化物酶(GPx-mimic)“四酶合一”催化活性。由於具有高比表面積和豐富的活性位點,表現出較高的催化效率📜。此外👨🏻🦽,FeIIITA塗層響應酸性環境而降解👃🏽,而不損害其類酶催化活性🪄。PdPtAu@TF作為納米反應器🏋🏽♀️,有潛力通過級聯催化反應重編程腫瘤營養和氧化還原代謝(圖2)💇🏻♂️。
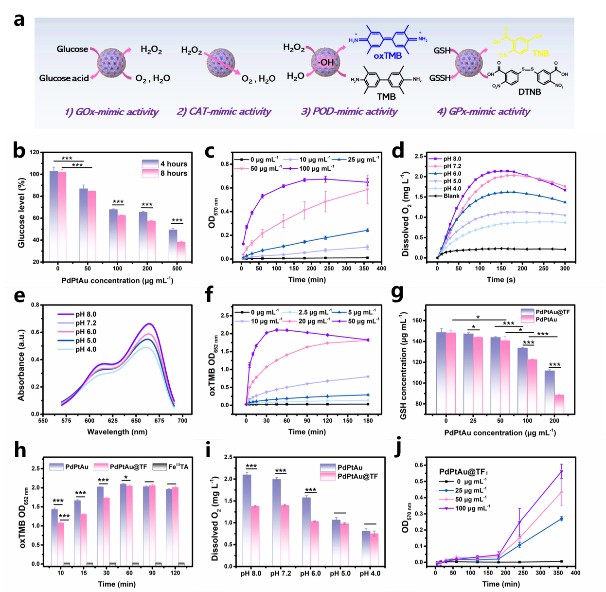
圖2:PdPtAu和PdPtAu@TF納米顆粒的類酶性質
細胞實驗結果表明,PdPtAu@TF可以與癌細胞競爭葡萄糖,將其轉化為過氧化氫🌷,使細胞陷入“饑餓”狀態👩🏼🏫,進而增強對“儲備能源”脂質的攝取和利用。同時,在細胞內催化過氧化氫分解生成活性氧和氧氣,消耗抗氧化劑谷胱甘肽🛞♥︎,從而誘導癌細胞落入鐵死亡陷阱💂🏼,增敏放射治療🌵。此外,由於腫瘤微環中過氧化氫的提高,促進了巨噬細胞向M1表型極化,有助於克服免疫抑製,增強抗腫瘤治療(圖3)🩵。
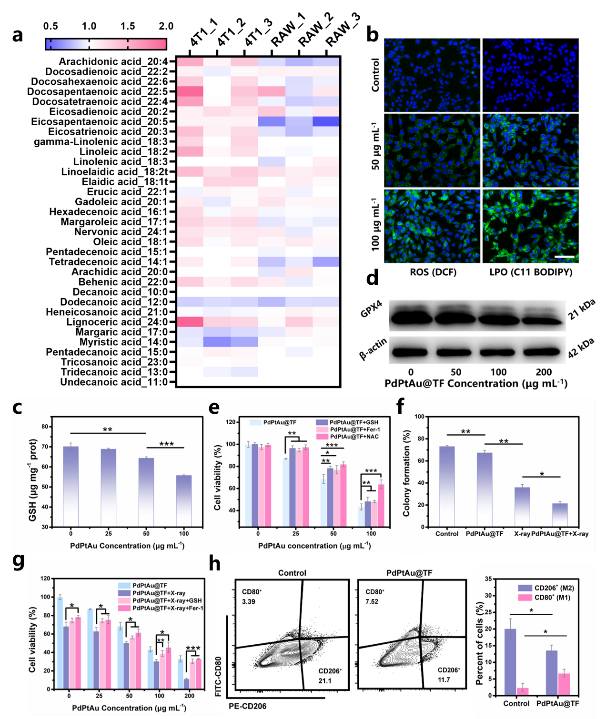
圖3🎬:PdPtAu@TF對癌細胞和巨噬細胞的代謝重編程作用
體內抗腫瘤實驗表明,PdPtAu@TF可以在小鼠體內誘導腫瘤鐵死亡並改善腫瘤乏氧🌠,使癌細胞對放療更加敏感。與對照組相比,單獨PdPtAu@TF治療或X射線治療均能抑製腫瘤生長Ⓜ️,但PdPtAu@TF與放療聯合的治療顯示出最突出的抗腫瘤效果(圖4)。

圖4:PdPtAu@TF聯合放療的抗腫瘤治療效果
同時,放療能夠有效激活小鼠免疫應答,PdPtAu@TF治療在促進巨噬細胞向M1表型極化中發揮重要作用🕵🏻♂️,而PdPtAu@TF聯合放療觸發了較單一治療更強的抗腫瘤免疫反應,能夠系統地調節適應性免疫和先天免疫,將免疫“冷”腫瘤轉化為“熱”腫瘤🤸🏿♀️,抑製轉移竈的發生。
更為重要的是🧑🏿✈️,平衡炎症反應介導的免疫激活和組織纖維化是克服放療抵抗的一大挑戰🌆,PdPtAu@TF納米酶聯合放療的治療策略在激活免疫應答的同時,抑製了癌症相關成纖維細胞的增殖和組織纖維化的形成,並成功抑製了腫瘤轉移(圖5)。
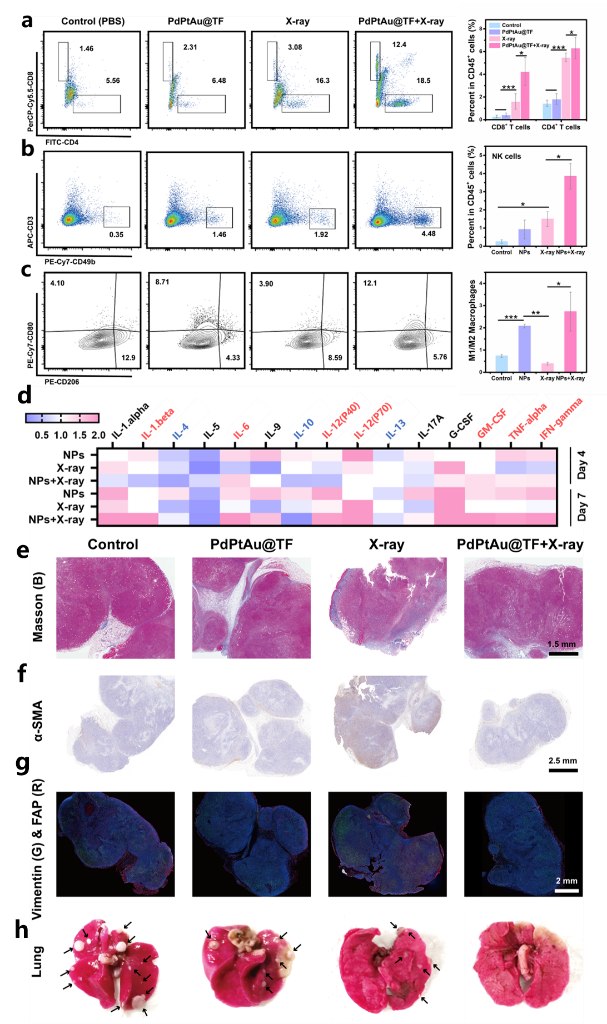
圖5:腫瘤免疫應答與CAFs增殖分析
綜上,本研究靶向癌症代謝的靈活性和可塑性,通過類酶催化反應重編程腫瘤營養和氧化還原代謝,顯著增強了放射免疫治療的效果,也為抗癌治療提供了一種新的思路。